
Ideando
prospero futuro

un

Clasificación del agua
De acuerdo a la concentración de carbonatos en el agua, ésta puede clasificarse en nivles de dureza, lasiguiente tabla indica las cantidades de sales.


Dureza del agua
El término dureza se define como la concentración de todos los cationes metálicos no alcalinos presentes (iones de calcio, estroncio, bario y magnesio en forma de carbonatos o bicarbonatos) y se expresa en equivalentes de carbonato de calcio y contituye un parámetro muy significativo en la calidad del agua.. Esta cantidad de sales afecta la capacidad de formación de espuma de detergentes en contacto con agua y representa una serie de problemas de incrustación en equipo industrial y dompestico, además de resultar nosiva para el consumo humano.
El agua adquiere la dureza cuando pasa a través de las formaciones geológicas que contienen los elementos minerales que la producen y por su poder solvente los disuelve e incorpora. El agua adquiere el poder solvente, debido a las condiciones ácidas que se desarrollan a su paso por la capa de suelo, donde la acción de las bacterias genera CO2, el cual existe en equilibrio con el ácido carbónico. En estas condiciones de pH bajo, el agua ataca las rocas, particularmente a la calcita (CaCO3), entrando los compuestos en solución.
El carbonato cálcico (CaCO3) es el carbonato más importante, que se presenta en la naturaleza como caliza, mármol y, en estado puro, como calcita. El CaCO3 se produce como precipitado difícilmente soluble al pasar CO2 a través de una disolución de hidróxido cálcico, así como durante el fraguado del mortero de cal, que es una mezcla de arena, cal apagada [Ca (OH)2] y agua:
Ca2+ + 2OH- + CO2 → CaCO3 (Precipitado) + H2O
Otros minerales importantes del tipo de los carbonatos son la dolomita (Ca, Mg)CO3, en el que la mitad de los iones Ca2+ han sido sustituido por iones Mg2+ y además el carbonato de zinc, el carbonato de manganeso y el carbonato de hierro. Los últimos constituyen minerales valiosos.
La calcita es un mineral que puede cristalizar en varias formas dando lugar a cristales generalmente blancos o incoloros, pero que a veces están teñidas de otras coloraciones. Su nombre viene del latín Calx, que significa cal viva. Es el mineral más estable que existe de carbonato de calcio, frente a los otros dos polimorfos con la misma fórmula química aunque distinta estructura cristalina: el aragonito y la vaterita, más inestables y solubles.
¿Cómo el agua adquiere la dureza?


Fragmento de calcita
Calcita que se formó por precipitación a partir del agua que circulaba por una grieta de la roca arenisca.

La dureza que se debe a los bicarbonatos y carbonatos de calcio y magnesio se denomina dureza temporal y puede eliminarse por ebullición, que al mismo tiempo esteriliza el agua.
Otra forma de explicarlo, cuando la dureza es numéricamente mayor que la suma de las alcalinidades de carbonatos y bicarbonatos, la cantidad de dureza que es su equivalente a esta suma se le llama dureza carbonatada, también llamada temporal, ya que al elevarse la temperatura del agua hasta el punto de ebullición, el calcio y el magnesio se precipitan en forma de carbonato de calcio e hidróxido de magnesio respectivamente.
La dureza temporal también puede ser eliminada por la adición del hidróxido de calcio (Ca(OH)2).
El carbonato de calcio es menos soluble en agua caliente que en agua fría, así que al hervir (que contribuye a la formación de carbonato) se precipitará el bicarbonato de calcio fuera de la solución, dejando el agua menos dura.
Los carbonatos pueden precipitar cuando la concentración de ácido carbónico disminuye, con lo que la dureza temporal disminuye, y si el ácido carbónico aumenta puede aumentar la solubilidad de fuentes de carbonatos, como piedras calizas, con lo que la dureza temporal aumenta. Todo esto está en relación con el pH de equilibrio de la calcita y con la alcalinidad de los carbonatos. Este proceso de disolución y precipitación es el que provoca las formaciones de estalagmitas y estalactitas.
Dureza temporal
Dureza permanente
La dureza residual se conoce como dureza no carbónica o permanente. La dureza permanente no puede ser eliminada al hervir el agua, es usualmente causada por la presencia del sulfato de calcio y magnesio y/o cloruros en el agua, que son más solubles mientras sube la temperatura hasta cierto valor, luego la solubilidad disminuye conforme aumenta la temperatura. Puede ser eliminada utilizando el método SODA (sulfato de sodio).
Otra explicación es que la cantidad de dureza en exceso de la carbonatada se le llama dureza de no carbonatos y se distingue como permanente, es decir, no puede eliminarse por agitación térmica, sino que son necesarios procesos químicos para eliminarla del agua.
Las aguas que poseen esta dureza pueden ablandarse añadiendo carbonato de sodio y cal, o filtrándolas a través de ceolitas naturales o artificiales que absorben los iones metálicos que producen la dureza, y liberan iones sodio en el agua. Los detergentes contienen ciertos agentes separadores que inactivan las sustancias causantes de la dureza del agua.
El hierro, que produce un sabor desagradable en el agua potable, puede extraerse por medio de la ventilación y sedimentación, o pasando el agua a través de filtros de ceolita. También se puede estabilizar el hierro añadiendo ciertas sales, como los polifosfatos. El agua que se utiliza en los laboratorios, se destila o se desmineraliza pasándola a través de compuestos que absorben los iones.




Tratamiento del agua dura
Los fines principales perseguidos con el tratamiento del agua son los siguientes:
1.- Quitar las materias solubles y en suspensión.
2.- Eliminación de los gases.
Todo esto es necesario, entre otras cosas para:
1.- Evitar la formación de incrustaciones sobre las superficies de calentamiento del agua.
2.- Proteger contra la corrosión los metales de las calderas, recuperadores y tuberías.
El proceso del tratamiento del agua incluye la separación de los detritos mediante mallas móviles o fijas, filtrado, separación de lodos y limos en depósitos de decantación, calentamiento, vaporización o destilación, desaireación, tratamiento con cal apagada, tratamiento con carbonato sódico, tratamiento con ambos productos, con hidróxidos cálcico y bárico, con fosfato trisódico, coagulantes, zeolitas (descalcificadoras) y por osmosis inversa.
Cuando el agua contiene una cantidad significante de calcio y magnesio, es llamada agua dura, la cual es conocida por taponar las tuberías y complicar la disolución de detergentes en agua. El ablandamiento del agua es una técnica que sirve para eliminar los iones que hacen a un agua ser dura, en la mayoría de los casos iones de calcio y magnesio. En algunos casos iones de hierro también causan dureza del agua. Iones de hierro pueden también ser eliminados durante el proceso de ablandamiento. El mejor camino para ablandar un agua es usar una unidad de ablandamiento de aguas y conectarla directamente con el suministro de agua.
Ablandamiento del agua
Los ablandadores de agua son específicos intercambiadores de iones que son diseñados para eliminar iones, los cuales están cargados positivamente. Los ablandadores mayormente eliminan los iones de calcio (Ca2+) y magnesio (Mg2), conocidos como minerales duros. Los ablandadores son algunas veces incluso aplicados para eliminar hierro, cuando el hierro causa la dureza del agua. Los mecanismos de ablandamiento son capaces de eliminar más de cinco miligramos por litro (5 mg/l) de hierro disuelto. Los ablandadores pueden operar de forma automática, semiautomática, o manual. Cada tipo tiene un ratio de actuación. Un ablandador de agua colecta los minerales que causan la dureza y los contiene en un tanque colector y este es de vez en cuando limpiado de su contenido. Intercambiadores iónicos son a menudo usados para ablandar el agua. Cuando un intercambiador iónico es aplicado para ablandar el agua, este reemplazará los iones de calcio y magnesio por otros iones, por ejemplo sodio y potasio. Los intercambiadores iónicos son añadidos desde un tanque de intercambiadores de iones que contiene sales de sodio y potasio. (NaCl y KCl).
Explicación química
sales que ablandan
Para ablandar el agua, tres tipos de sales se venden generalmente
:1. Sal de roca
2. Sal solar
3. Sal evaporada
La sal de roca como mineral ocurre naturalmente en la tierra. Es obtenida de depósitos subterráneos por métodos tradiciones de minería. Contienen entre el noventa y ocho y noventa y nueve por ciento de cloruro de sodio. Tiene un nivel de insolubilidad en agua de cerca de 0,5-1,5% siendo principalmente sulfato cálcico. Su componente más importante es sulfato de calcio. La sal solar como producto natural se obtiene principalmente con la evaporación del agua de mar. Contiene cloruro de sodio al 85%. Tiene un nivel de insolubilidad en agua de menos de 0,03%. Se vende generalmente en forma cristalina. También se vende a veces en pelotillas. La sal evaporada se obtiene a través de procesos de minería de depósitos subterráneos que contienen la sal, esta sal se disuelve. La humedad se evapora, usando energía como es el gas natural o el carbón. La sal evaporada contiene cloruro de sodio entre un 99,6 y 99,99%.
Ablandamiento del agua
Las compañías productoras de agua tienen la oportunidad de producir agua blanda, sin embargo no siempre lo hacen así. Una compañía productora de agua solo tiene que añadir al agua un ablandador en su sistema de purificación, para producir agua blanda barata.
Los problemas del agua dura ocurren mayormente cuando el agua es calentada. Como resultado, el agua dura causa algunos problemas en los suministros de agua de las compañías, especialmente cuando solo el agua fría corre a través de las tuberías.
El agua ablandada todavía contiene todos los minerales naturales que necesitamos. Se priva solamente de su contenido en calcio y en magnesio, el sodio es añadido en el proceso de ablandamiento. Ése es porqué en la mayoría de los casos, el agua ablandada es perfectamente segura de beber. Es recomendable que como agua ablandada contenga solamente hasta 300mg/L de sodio. En áreas con aguas de alta dureza y que es ablandada no debe de usarse para preparar la leche de los niños, debido al alto contenido en sodio que se produce por el proceso de ablandamiento llevado a cabo.
La toma de sodio a través del agua ablandada depende de la dureza del agua. Como media, la toma de sodio es menos del 3% que viene de beber el agua ablandada.Las estimaciones dicen que una persona consume cerca de dos a tres cucharillas de sal al día, de varias fuentes. Si se asume que un producto diario de cinco gramos de sodio a través del alimento y de la consumición de tres cuartos de galón de agua, la contribución del sodio (Na+) en el agua del proceso casero el ablandar el agua, es mínima comparada al producto diario del total de muchos alimentos ricos en sodio.
Funciona agregando el agua a través de un lecho de iones con carga negativa que atraen los iones de magnesio y calcio que contienen las aguas duras. La presencia del sodio en el agua puede resultar perjudicial para la salud, por lo que a veces se recomienda disponer de una segunda línea de bebederos para poner adentro. La cantidad de sodio absorbido a través de éste sistema depende de la dureza del agua que está siendo filtrada.
Ablandadores de sal para el agua
En situaciones en las que el sodio no puede ingresar en los organismos de las personas, se recomienda utilizar suavizantes sin sal, en los cuales el agua se extrae a través de las perlas de resina de cloruro de potasio, quedando el magnesio y el calcio desactivados.
Ablandadores de agua sin sal
Los suavizadores de agua electrónicos funcionan mediante la desactivación de la electrónica de los iones de magnesio y calcio. Estos se instalan alineados con el abastecimiento de agua y no necesitan mantenimiento. Por desgracia, no parecen funcionar bien en áreas con altas cantidades de hierro en el agua, por lo que vale la pena probar el agua primero. Los imanes también se han estudiado como una posibilidad para este problema, pero muchos consideran que esto es menos eficaz para ablandar el agua que es muy dura.
El agua dura debe de ser tratada, es decir, hacerla más suave y eliminar los minerales que contiene. Al suavizar el agua, los usos de esta incrementan y se evitan problemas con aparatos y tuberías. La forma más convencional de suavizar el agua depende de un proceso de intercambio de iones, para de esta manera eliminar los minerales. En los aparatos para lograr esto se tiene una capa de cuentas saturadas con sodio que retienen los minerales y después son eliminadas.Los tratamientos para el agua dura se pueden dar en varios niveles, uno de estos es el hogar. Los aparatos que suavizan el agua se pueden clasificar en los siguientes cuatro tipos:
Manuales: en el cual el dueño hace cada uno de los pasos para recargar la unidad de intercambio de iones.
Semi automático: en el cual el dueño empieza manualmente el proceso, excepto la terminación automática de limpiado y regreso a la fuente.
Automático: en el cual el dueño detiene la unidad cuando se necesiten recargar las cuentas. Todos los pasos después se hacen de manera automática.
Completamente automático: en el cual la unidad funciona con reloj y todas las operaciones se activan automáticamente. El material que contiene el sistema sirve para varias funciones, pero se tienen que cambiar cuando se indique.
Suavizadores de agua magnéticos y electrónicos
EFECTOS EN EL ECOSISTEMA
El agua dura es aquella que contiene una considerable cantidad de minerales disueltos en ella, se produce de forma natural en los estaques que no son formados por intervención del hombre. Estos estanques naturales son cuerpos de agua más pequeños que los lagos. El agua dura es útil para la vida animal y vegetal en un estanque. La Agencia de protección del ambiente de los Estados Unidos recomienda que el agua potable tenga un pH de entre 6.5 a 8.5. Aunque es sana para el cuerpo, los minerales como el calcio pueden causar problemas con su posicionamiento en superficies de cerámica y por su gusto agrio. Los depósitos minerales en las bañeras y los dispositivos del hogar pueden dejar residuos en escamas.
El agua dura contiene niveles altos de calcio y magnesio, entre más cantidad de estos minerales que tenga, más dura se hace el agua. No es mala para la salud, pero si puede causar problemas con las tuberías. Suele causar la acumulación de minerales en la tubería de agua y sistemas de calefacción, y su pobre rendimiento con el jabón o detergentes en comparación con agua blanda.
El agua es un buen solvente y toma impurezas fácilmente. Como el agua se mueve a través de suelo y roca, disuelve los minerales y los mantiene en solución. El calcio y el magnesio disueltos en el agua son los dos minerales más comunes que hacen el agua "dura". El grado de dureza es mayor a medida que aumenta el contenido del calcio y el magnesio.




pH y Alcalinidad
Medida de calidad de agua: el pH
El pH es un factor muy importante, porque determinados procesos químicos solamente pueden tener lugar a un determinado pH.
El pH es un indicador de la acidez de una sustancia. Está determinado por el número de iónes libres de hidrógeno (H+) en una sustancia.
La acidez es una de las propiedades más importantes del agua. El agua disuelve casi todos los iones. El pH sirve como un indicador que compara algunos de los iones más solubles en agua. El resultado de una medición de pH viene determinado por una consideración entre el número de protones (iones H+) y el número de iones hidroxilo (OH-). Cuando el número de protones iguala al número de iones hidroxilo, el agua es neutra. Tendrá entonces un pH alrededor de 7. El pH del agua puede variar entr 0 y 14. Cuando el ph de una sustancia es mayor de 7, es una sustancia básica. Cuando el pH de una sustancia está por debajo de 7, es una sustancia ácida. Cuanto más se aleje el pH por encima o por debajo de 7, más básica o ácida será la solución. El pH es un factor logarítmico; cuando una solución se vuelve diez veces más ácida, el pH disminuirá en una unidad. Cuando una solución se vuelve cien veces más ácida, el pH disminuirá en dos unidades.El término común para referirse al pH es la alcalinidad.
Métodos de determinación del pH
Existen varios métodos diferentes para medir el pH. Uno de estos es usando un trozo de papel indicador del pH. Cuando se introduce el papel en una solución, cambiará de color. Cada color diferente indica un valor de pH diferente. Este método no es muy preciso y no es apropiado para determinar valores de pH exactos. Es por eso que ahora hay tiras de test disponibles, que son capaces de determinar valores más pequeños de pH, tales como 3.5 o 8.5. El método más preciso para determinar el pH es midiendo un cambio de color en un experimento químico de laboratorio. Con este método se pueden determinar valores de pH, tales como 5.07 y 2.03.
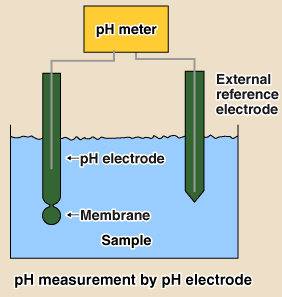
El electrodo de pH
Un electrodo de pH es un tubo el cual Está unido a un pH-metro por medio de un cable. Un tipo especial de fluído se coloca dentro del electrodo. Algunos electrodos contienen un gel que tiene las mismas propiedades que el fluído 3M. En el fluído hay cables de plata y platino. El sistema es bastante frágil, porque contiene una pequeña membrana. Los iones H+ y OH- entrarán al electrodo a través de esta membrana. Los iones crearán una carga ligeramente positiva y ligeramente negativa en cada extremo del electrodo. El potencial de las cargas determina el número de iones H+ y OH- y cuando esto haya sido determinado el pH aparecerá digitalmente en el pH-metro. El potencial depende de la temperatura de la solución. Es por eso que el pH-metro también muestra la temperatura.
ácidos y bases
Cuando los ácidos entran en contacto con el agua, los iones se separan. Por ejemplo, el cloruro de hidrógeno se disociará en iones hidrógeno y cloro (HCL--à H+ + CL-). Las bases también se disocian en sus iones cuando entran en contacto con el agua.
Cuando el hidróxido de sodio entra en el agua se separará en iones de sodio e hidroxilo (NaOH--à Na+ + OH-). Cuando una sustancia ácida acaba en el agua, le cederá a ésta un protón. El agua se volverá entonces ácida. El número de protones que el agua recibirá determina el pH. Cuando una sustancia básica entra en contacto con el agua captará protones. Esto bajará el p del agua. Cuando una sustancia es fuertemente ácida cederá más protones al agua. Las bases fuertes cederán más iones hidroxilo.








Ventajas
Desventajas
El agua dura con el contenido mineral puede prevenir las enfermedades del corazón, baja la presión arterial y hace los huesos más fuertes y mejores con la ingesta de calcio. Generalmente el agua dura es mucho más recomendable
El agua dura, por lo contrario al agua blanda no permite el ahorro de dinero. Cuando el agua es blanda, usa mucho menos jabón y menos productos de limpieza.
La plomería no durará mucho tiempo. El agua dura puede causar la acumulación de sarro y depósitos minerales. Con el tiempo, las tuberías se pueden tapar y el flujo de agua puede disminuir. Esto no pasa con el agua blanda.
El calentador de agua durará más tiempo. La acumulación de sarro y depósitos de calcio creados por los minerales se llevará a cabo con el agua dura. Esto agrega vida a su calentador de agua, costará aproximadamente 20% mas calentar el agua que usa la familia.
La mayoría de los aparatos que usan agua dura, no durarán mucho tiempo. Ya sea la cafetera, el humidificador, la bañera o yacusi, el agua dura propiciará la acumulación de minerales y quitará vida a estos productos.
La ropa durará menos y perderá la fuerza de los colores. La razón es que el agua dura deja partículas minerales en el tejido de la mayoría de las telas. Esto ocasiona que estas se ven opacas y desgastadas. También, la lavadora automática durará menos, porque estará sujeta a la acumulación y depósito de minerales.
Habrá anillos de sarro y manchas en los muebles, llaves y grifos del baño.Los vasos y platos tendrán rayas blancas de calcio.Tallar el piso y los mosaicos será mucho más difícil y lento, ya que quedará una película de residuos de jabón que se forman con el agua dura
Bibliografía
-
www.quimica.uc.cl/uploads/commons/images/f_agua%20dura.pdf
-
iesfgcza.educa.aragon.es/depart/.../TrabajoNavidades2007.pdf
-
catarina.udlap.mx/u_dl_a/tales/documentos/leip/...m.../capitulo3.pdf
-
www.tucsonaz.gov/files/water/docs/Hard_Water_Spanish_6_7_2013.pdf
-
quimica.laguia2000.com/conceptos-basicos/aguas-duras-y-blandas
-
http://www.investigacion.frc.utn.edu.ar/sensores/PH/pH.htm
-
http://www.lenntech.es/ph-y-alcalinidad.htm